A) Metabolitos polioxigenados a partir de sintones de origen microbiano
Investigadores responsables: Gustavo Seoane, Margarita Brovetto
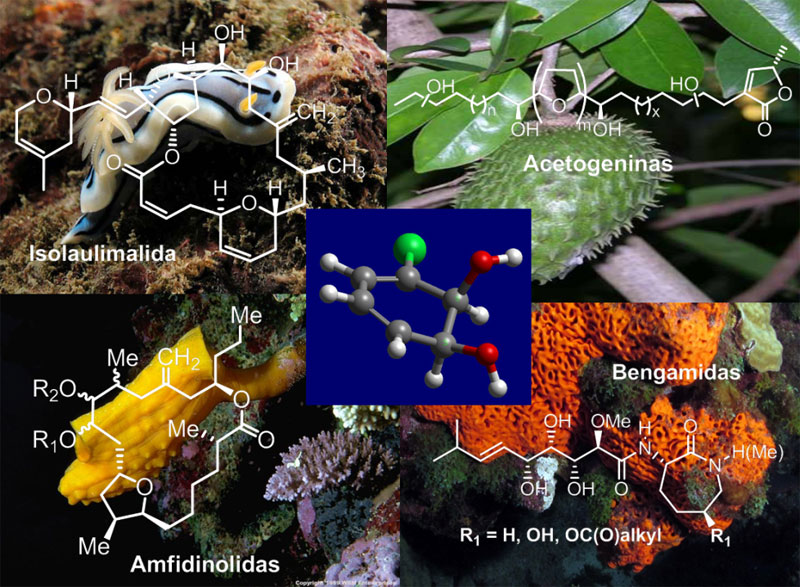
La química de los productos naturales, tanto de origen marino como terrestre, ha jugado un papel especialmente importante dentro de la química orgánica, debido a la alta diversidad de moléculas aislables y a su amplio espectro de actividad biológica. La disponibilidad limitada de sus fuentes naturales y la necesidad de contar con una cantidad apreciable de muestra para los distintos ensayos biológicos, hace imperioso el desarrollo de procedimientos eficientes de síntesis. La línea de investigación busca la preparación de compuestos naturales o análogos mediante procedimientos enantioselectivos, combinando estrategias quimioenzimáticasy de síntesis orgánica clásica estéreo- y enantioselectiva.
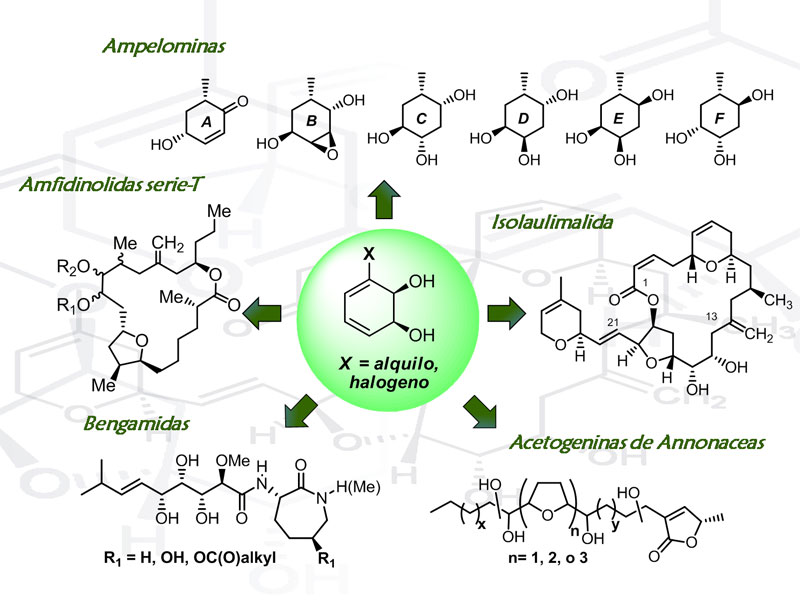
Los métodos enzimáticos usados se basan fundamentalmente en la biotransformación de compuestos aromáticos simples para formar dioles homoquirales, los cuales se emplean como materiales de partida en las secuencias sintéticas. Estos dioles, obtenidos por dihidroxilación de aromáticos mediada por dioxigenasas bacterianas,1 se han usado en aproximaciones sintéticas a diversos compuestos polioxigenados, como Bengamidas, Isolaulimalida, oligotetrahidrofuranos análogos a acetogeninas naturales, Amfidinolidas de la serie-T, Ampelominas, δ-lactonas insaturadas, y otros.2 Entre las ventajas de esta metodología se cuenta una elevada enantioselectividad y un menor impacto ambiental, lo que hace que estos métodos se clasifiquen dentro de la química verde o sustentable.
Como forma complementaria a la síntesis se ensayan las actividades biológicas (ensayos de actividad antitumoral, antiproliferativa, antihelmíntica, según corresponda) de los productos finales y de los intermedios obtenidos a lo largo de la investigación.
-
-
- Martín, T., Rodríguez-López, J., Brovetto, M., & Martín, V. S.Enantiodivergent cyclization by inversion of the reactivity in ambiphilic molecules Angewandte Chemie International Edition, 2020, 59, 17077-17083, DOI:10.1002/anie.202006650.
- B”, Brindisi, C.; Vazquez, S.; Suescun, L.; Seoane, G.; Martín, V.; Brovetto, M Chemoenzymatic Total Synthesis and Structural Revision of Ampelomins B, D, E, and epi-Ampelomin J. Org. Chem. 2019, 84, 15997–16002. doi: 10.1021/acs.joc.9b02472
- “RedoxBiocatalysis: Fundamentals and Applications”, Gamenara, D.; Seoane, G. A.; Saenz-Méndez, P; Domínguez de María, P. J. Wiley&Sons: Hoboken, NJ, USA, 2013, capítulo 4, pág. 251-274.
- a) “Chemoenzymatic synthesis of enantiopureα-substituted cyclohexanones from aromatic compounds”, Fonseca, G.; Seoane, G. Tetrahedron: Asymmetry, 2005, 16(7), 1393-1402; b) “Stereoselective Synthesis of 3-Oxygenated-cis-dialkyl-2,5-substituted Tetrahydrofurans from Cyclohexadienediols” Brovetto, M.; Seoane, G. J. Org. Chem. 2008, 73, 5776-5785; c) “Chemoenzymatic Synthesis of trans-Tetrahydrofuran Cores of AnnonaceousAcetogenins from Bromobenzene”. Ramos, J.-C.; Brovetto, M.; Seoane, G. Org. Lett.2013, 15, 1982-1985; d) “Chemoenzymatic preparation of (6R)-5,6-dihydro-2H-pyran-2-one: an ubiquitous structural motif of biologically active lactones”. Carrera, I.; Brovetto, M.; Seoane, G. Tetrahedron: Asymmetry2013, 24, 1467-72; e) “Stereoselective hydrogenation of methylcyclohex-2-ene-1,4-diols used in the synthesis of ampelomins and deoxy-carbasugars”. Lagreca, M.E.; Carrera, I.; Seoane, G.A.; Brovetto, M. Tetrahedron Letters 2014, 55, 853-6; f) “Symmetry-based design for the chemoenzymatic synthesis of Oseltamivir (Tamiflu) from ethyl benzoate”Sullivan, B.; Carrera, I.; Drouin, M.; Hudlicky, T Angew. Chem. Int. Ed. 2009, 48, 4229-4231.
-
Proyectos asociados
-
- “Chemoenzymatic synthesis of C6-C13 fragment of Amphidinolide T- Series” Financiado por: Organization for the Prohibition of Chemical Weapons (OPCW). Período 2015-2017. Responsable: Margarita Brovetto. Monto financiado:€ 25.000.
-
- “Desarrollo de compuestos bioactivos. Exploración de nuevas metodologías sintéticas” Financiado por convocatoria I-COOP+ 2014 del Ministerio de Economía y Competitividad, del Gobierno Español Proyecto CSIC Tenerife, España- FQ, UdelaR. ). Período 2015-2017. Responsable: Margarita Brovetto. Monto financiado:€ 20.000.
- Oligo-tetrahidrofuranos 2,5-disustituidos. Síntesis quimioenzimática y evaluación biológica, financiado por CSIC-803, 2013-2014.
- Síntesis quimioenzimática y evaluación biológica de oligotetrahidrofuranos análogos a acetogeninas naturales, financiado por FCE 2009-3094, 2010-2012.
- Biotransformación de aromáticos en la preparación de isolaulimalida, financiado por PDT, 2006-2007.
- Síntesis y evaluación biológica de bengamidas y derivados mediante biotransformaciones, financiado por CSIC-299, 2005-2006.
- Aproximación quimioenzimática a la síntesis del fragmento C6-C13 de Amfidinolidas de la serie-TFinanciación: CSIC, Modalidad: Iniciación a la Investigación, 2010-2011.
Publicaciones
-
-
- “Tetrahydrofuran Formation through Intramolecular Iodoetherification: Mechanistic Insights into the Neighbouring-Group Participation of an Ester” Veiga, N.; Ramos, J. C.; Seoane, G.; Brovetto, M. European Journal of Organic Chemistry. 2017, 26, 3856-3859.
- “Concise Preparation of the Bis-THF Core of Annonaceous Acetogenins”, Delgue, E.; Brovetto, M.; Seoane, G. Synthesis 2016; 48(23): 4110-4116,
- “Structural Factors of Annonaceous Acetogenins and Their Semisynthetic Analogues Related with the Toxicity on Spodoptera frugiperda” Di Toto Blessing, L.; Budeguer, F.; Ramos, J.; Bardón, A.; Diaz, S.; Brovetto, M.; Seoane, G.; Neske, A. Journal of Agricultural Chemistry and Environment, 2015, 4, 56-61
- “Stereoselective hydrogenation of methylcyclohex-2-ene-1,4-diols used in the synthesis of ampelomins and deoxy-carbasugars”, Lagreca, M.E.; Carrera, I.; Seoane, G.; Brovetto, M. Tetrahedron Letters 2014, 55, 853–856.
-
-
-
- “Chemoenzymatic preparation of (6R)-5,6-dihydro-2H-pyran-2-one:a ubiquitous structural motif of biologically active lactones” Carrera, I.; Brovetto, M.; Seoane, G. Tetrahedron: Asymmetry 2013, 24,1467–1472.
-
-
-
- “Chemoenzymatic Synthesisof trans-Tetrahydrofuran Coresof Annonaceous Acetogeninsfrom Bromobenzene”. Ramos, J.C.; Brovetto, M.; Seoane, G.Org. Lett. 2013, 15 (8), 1982-1985.
-
-
-
- “Insecticidal Properties of AnnonaceousAcetogenins and TheirAnalogues.Interaction with Lipid Membranes”. Di Toto Blessing, L.; Ramos,J.C.; Diaz, S.; Ben Altabef, A.; Bardón, A.; Brovetto, M.; Seoane, G.; Neske, A. Natural Product Communications 2012, 7 (9), 1215-1218.
-
-
-
- “Several Generations of Chemoenzymatic Synthesis of Oseltamivir (Tamiflu): Evolution of Strategy, Quest for a Process-Quality Synthesis, and Evaluation of Efficiency Metrics” Werner, L.; Machara, A.; Sullivan, B.; Carrera, I.; Moser, M.; Adams, D .R.; Hudlicky, T. J. Org. Chem. 2011, 76, 10050-10067.
-
-
-
- “Microwave-assisted, solvent-free oxidative cleavage of a-hydroxyketones”. Carrera, I.; Brovetto, M.; Ramos, J.C.; Seoane, G. Tetrahedron Letters 2009, 50,5399–5402.
-
-
-
- “Symmetry-based design for the chemoenzymatic synthesis of Oseltamivir (Tamiflu) from ethyl benzoate”Sullivan, B.; Carrera, I.; Drouin, M.; Hudlicky, TAngew. Chem. Int. Ed. 2009, 48, 4229-4231
-
-
-
- “Stereoselective Synthesis of 3-Oxygenated-cis-dialkyl-2,5-substituted Tetrahydrofurans from Cyclohexadienediols”. Brovetto, M.; Seoane, G. J. Org. Chem.2008, 73, 5776–5785.
-
B) Oxociclaciones enantioselectivas
Investigadora responsable: Margarita Brovetto
Los éteres ciclos de diferentes tamaños están presentes en una amplia y variada gama de productos naturales con diversa actividad biológica (antitumoral, antihelmíntica, antimalárica, antimicrobiana etc.) y representan bloques quirales muy versátiles para la síntesis enantioespecífica de muchos compuestos naturales. En especial, los éteres policíclicos de origen marino han atraído el interés de la comunidad científica debido a su compleja estructura y a sus importantes actividades a nivel biológico.1 Las metodologías de síntesis de los mismos han sido muy variadas siendo las oxaciclaciones enantioselectivas una herramienta muy utilizada para la construcción de éteres de 5, 6 y más números de átomos en el ciclo.2
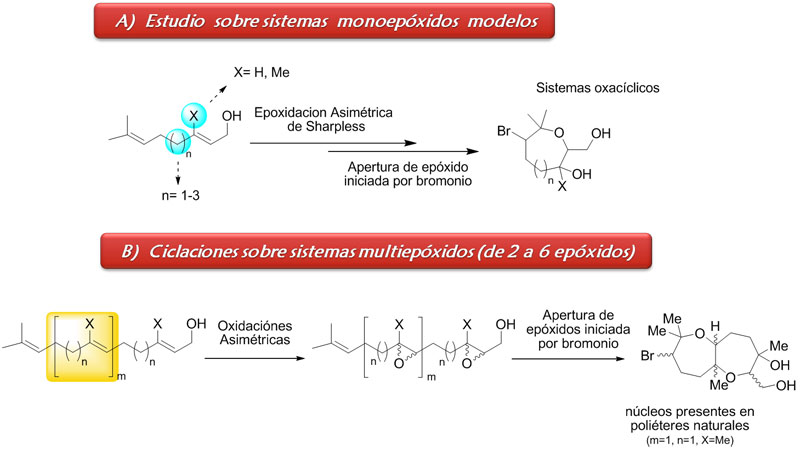
Esta línea de investigación, iniciada recientemente, estudia la formación de éteres cíclicos mediante la incorporación enantioselectiva de funciones oxigenadas a sistemas polienos, las cuales se utilizan posteriormente para los estudios de oxaciclación. Las diferentes estereoquímicas de las funciones oxigenadas así como las metodologías de oxaciclación a ensayar permiten realizar un estudio sistemático hacia la construcción de sistemas polioxigenados cíclicos. Las metodologías de oxidación enantioselectivas que se utilizan implican epoxidaciónes asímetricas de Sharpless, dihidroxilaciones asímetricas de Sharpless, epoxidaciónes de Shi entre otras; y las oxaciclaciones en estudio involucran aperturas de epóxidos mediadas por la formación de centros electrofílicos en los sistemas polienos hidroxilados.3 El estudio implica partir de sistemas polienos naturales de 2, 3 y hasta 6 dobles enlaces, estudiando en forma sistemática como influyen las diferentes estereoquímicas de las funciones oxigenadas, y las condiciones de oxaciclación a la formación de éteres cíclicos, buscando si es posible, patrones de comportamiento a nivel sintético.
El conocimiento generado se aplica a la síntesis de poliéteres de tipo terpenoides.
- a. Inoue, M. .Chem Rev.2005,105,4314-4347; b. Fernandez, J.J; Souto, M.L.; Norte M. Nat.Prod.Rep. 2000, 17, 235-246.
- a. Vilotijevic, I.; Jamison, T. Marine Drugs, 2012, 8, 763-809; b. Sasaki, M.; Fuwa, H. Nat.Prod.Rep. 2008, 47, 7182-7225.
- a. Underwood, B.S.; Tanuwidjaja, J.; Ng, S-S.; Jamison, T. Tetrahedron 2013, 69, 5205-5220.

